Lijst met elementen
»
actinium
»
argon
»
astatine
»
barium
»
bismut
»
bohrium
»
Borium
»
broom
»
cadmium
»
calcium
»
cerium
»
cesium
»
chloor
»
chromium
»
curium
»
dubnium
»
erbium
»
europium
»
fermium
»
fluorine
»
fosfor
»
francium
»
gallium
»
goud
»
hafnium
»
hassium
»
helium
»
holmium
»
ijzer
»
indium
»
iridium
»
jodium
»
kalium
»
kobalt
»
koolstof
»
koperen
»
krypton
»
lantaan
»
lithium
»
Lood
»
lutecium
»
mangaan
»
natrium
»
neon
»
Nihonium
»
nikkel
»
niobium
»
nobelium
»
osmium
»
platina
»
polonium
»
radium
»
radon
»
rhenium
»
rhodium
»
rubidium
»
rutenium
»
samarium
»
scandium
»
selenium
»
silicium
»
stikstof
»
tallium
»
tantalum
»
Tennesse
»
terbium
»
thorium
»
thulium
»
tin
»
titanium
»
uranium
»
vanadium
»
wolfraam
»
xenon
»
yttrium
»
Zilver
»
zink
»
zuurstof
»
zwavel
Cs - cesium - ALKALIMETAAL
Cesium is een metaal uit groep 1 van het periodiek systeem. Het chemische element is Cs en het heeft een atoomnummer van 55. De atoommassa is 132,905 g/mol en het smeltpunt is 28°C, waardoor het zeer kneedbaar is en een zeer lage dichtheid heeft. Het heeft een zilveren kleur en gloeit in het donker, wat het de bijnaam "glanzend metaal" opleverde.
cesium heeft zeer hoge reactieve eigenschappen. Het reageert heel gemakkelijk met zuurstof en water en kan bij kamertemperatuur zelfs reageren met koper. Het wordt in de industrie zeer veel gebruikt als katalysator in chemische processen, vooral tijdens de productie van aardolieproducten.
Vanuit medisch oogpunt wordt cesium gebruikt om verschillende ziekten te behandelen, waaronder kanker en de ziekte van Parkinson. Het wordt ook gebruikt als basischemicaliën bij de vervaardiging van medicijnen en farmaceutische verbindingen.
cesium wordt ook gebruikt in de elektronica-industrie vanwege zijn geleidende eigenschappen en zijn vermogen om alfadeeltjes te produceren. Het wordt veel gebruikt bij de vervaardiging van diodes, transistors en geïntegreerde schakelingen.
cesium wordt ook gebruikt in halogeenlampen en kunstwerken, waar het wordt gebruikt vanwege zijn uitzonderlijke thermische en galvanische eigenschappen. Metallurgie en de lucht- en ruimtevaartindustrie gebruiken cesium ook vanwege zijn mechanische en elektrochemische eigenschappen.
cesium heeft zeer hoge reactieve eigenschappen. Het reageert heel gemakkelijk met zuurstof en water en kan bij kamertemperatuur zelfs reageren met koper. Het wordt in de industrie zeer veel gebruikt als katalysator in chemische processen, vooral tijdens de productie van aardolieproducten.
Vanuit medisch oogpunt wordt cesium gebruikt om verschillende ziekten te behandelen, waaronder kanker en de ziekte van Parkinson. Het wordt ook gebruikt als basischemicaliën bij de vervaardiging van medicijnen en farmaceutische verbindingen.
cesium wordt ook gebruikt in de elektronica-industrie vanwege zijn geleidende eigenschappen en zijn vermogen om alfadeeltjes te produceren. Het wordt veel gebruikt bij de vervaardiging van diodes, transistors en geïntegreerde schakelingen.
cesium wordt ook gebruikt in halogeenlampen en kunstwerken, waar het wordt gebruikt vanwege zijn uitzonderlijke thermische en galvanische eigenschappen. Metallurgie en de lucht- en ruimtevaartindustrie gebruiken cesium ook vanwege zijn mechanische en elektrochemische eigenschappen.
Synthetisch
Radioactief
Vloeistof
Gasvormig
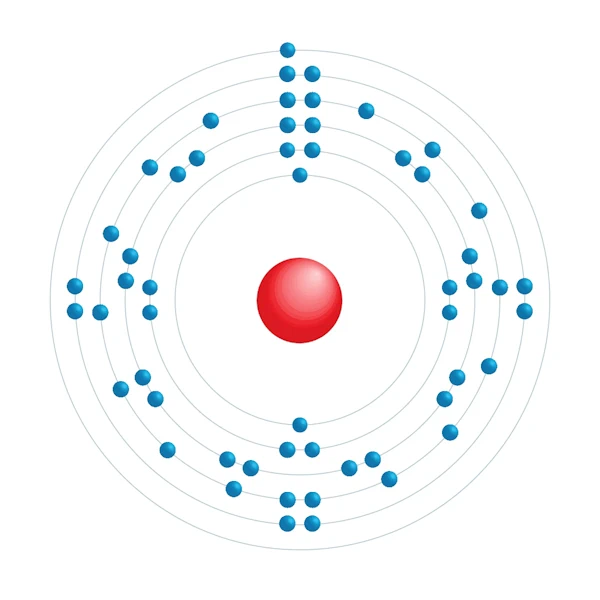
Elektronisch configuratiediagram
| Namn | cesium |
| Aantal | 55 |
| Atomair | 132.90545196 |
| Symbool | Cs |
| Fusie | 28.4 |
| Koken | 690 |
| Dichtheid | 1.873 |
| Periode | 6 |
| Groep | 1 |
| Ontdekking | 1860 Bunsen and Kirchoff |
| Overvloed | 3 |
| Straal | 3.3 |
| Elektronegativiteit | 0.79 |
| Ionisatie | 3.8939 |
| Aantal isotopen | 22 |
| Elektronische configuratie | [Xe] 6s1 |
| Oxidatie stelt | 1 |
| Elektron op energieniveau | 2,8,18,18,8,1 |
| Mineralen | Hardheid | Dichtheid |
| Avogadrite | 2.62 | |
| Caesiumpharmacosiderite | ||
| Cesiodymite | ||
| Cesplumtantite | 7.00 / 7.00 | 6.00 |
| Dachiardite-Ca | 4.00 / 4.50 | 2.14 |
| Gainesite | 4.00 / 4.00 | 2.94 |
| Galkhaite | 3.00 / 3.00 | 5.40 |
| Kirchhoffite | 6.00 / 6.50 | 3.64 |
| Kupletskite-(Cs) | 4.00 / 4.00 | 3.68 |
| Londonite | 8.00 / 8.00 | 3.34 |
| Margaritasite | 2.00 / 2.00 | 5.40 |
| Mccrillisite | 4.50 / 4.50 | 3.12 |
| Mendeleevite-(Ce) | ||
| Mendeleevite-(Nd) | 5.00 / 5.50 | 3.16 |
| Nalivkinite | 3.29 | |
| Nanpingite | 2.50 / 3.00 | 3.11 |
| Natrobistantite | 6.10 | |
| Odigitriaite | 5.00 / 5.00 | 2.83 |
| Pautovite | 2.50 / 2.50 | 3.85 |
| Pezzottaite | 8.00 / 8.00 | 2.97 |
| Pollucite | 6.50 / 6.50 | 2.90 |
| Potassicmendeleevite-(Ce) | ||
| Ramanite-(Cs) | ||
| Rhodizite | 8.50 / 8.50 | 3.44 |
| Senkevichite | 5.50 / 6.00 | 3.13 |
| Sokolovaite | ||
| Telyushenkoite | 6.00 / 6.00 | 2.73 |
| Zeravshanite | 6.00 / 6.00 | 3.09 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se